Dimissioni del primo paziente che ha ricevuto uno xenotrapianto di rene suino al MGH
- articolo del prof. Sergio Barocci
XENOTRAPIANTI RENALI

Tra il 1963 ed il 1964 il chirurgo statunitense della Tulane University, Keith Reemtsma, trapiantò dei reni di scimpanzè su nove pazienti, utilizzando la tecnica ‘en bloc‘, dove i due i reni con i vasi sanguigni che li accompagnano (comprese l’aorta e la vena cava) furono impiantati e uniti all’arteria iliaca esterna e alla vena iliaca esterna del ricevente. Una di questi pazienti riprese a lavorare e sopravvisse nove mesi all’intervento sottoponendosi a terapia immunosoppressoria con azatioprina e prednisolone. Si è scoperto che la sua morte per arresto cardiaco era dovuta a uno squilibrio di elettroliti, probabilmente a causa della minzione eccessiva osservata in seguito al trapianto di rene di scimpanzé. All’autopsia, sorprendentemente, i suoi reni trapiantati non mostrassero alcun segno di rigetto e apparirono normali.
Ma ben presto la tecnica fu abbandonata per le eccessive barriere immunologiche.
Negli ultimi anni, con i grandi sviluppi dell’ingegneria genetica, in modo particolare del CRISPR-Cas9, gli xenotrapianti stanno tornando di moda.
Al Massachusetts General Hospital
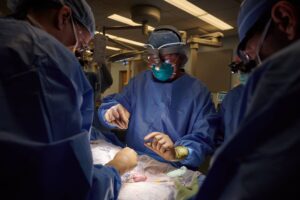
Il 16 marzo scorso è stata annunciata dall’équipe di trapianti del Massachusetts General Hospital (MGH) l’esecuzione del primo trapianto di rene al mondo in un essere umano da maiale geneticamente modificato. Ora, dopo poco più di due settimane, il paziente che è stato sottoposto a tale trapianto, è stato dimesso dall’ospedale e risulta finora star bene anche se aveva manifestato un rigetto cellulare otto giorni dopo l’intervento di trapianto.
E’ da tenere presente che questo rigetto non è neppure raro nei trapianti che vengono eseguiti da reni umani convenzionali, verificandosi, normalmente, in circa un quarto dei pazienti entro i primi tre mesi.
RIGETTO CELLULARE
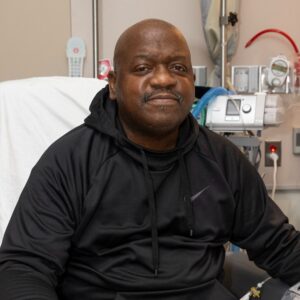
Infatti, dopo il trattamento con una globulina antitimocita (ATG) e un corticosteroide, la funzione renale del paziente è migliorata ed i livelli di creatinina sono tornati ai valori di base
Il paziente, Rick Slayman, un uomo di 62 anni, aveva avuto una lunga storia di diabete di tipo 2 e ipertensione arteriosa, e sviluppato una malattia renale allo stadio terminale (ESKD) dopo il fallimento di un precedente trapianto di rene da donatore cadavere umano nel 2018 presso lo stesso centro.
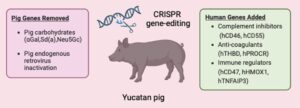
Durante l’intervento, durato 4 ore, a questo paziente è stato trapiantato un rene proveniente da un modello di suino donatore geneticamente modificato, utilizzando la tecnologia di editing genetico CRISPR-Cas9 per ingegnerizzare il modello suino in modo da apportare 69 modifiche genomiche che eliminerebbero gli zuccheri cellulari potenzialmente dannosi e inattiverebbero i virus che potrebbero causare un’infezione nell’uomo.
un suino donatore
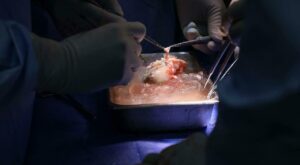
Tale modello suino è stato sviluppato nel corso di 5 anni in collaborazione tra il MGH e la eGenesis, di Cambridge, Massachusetts (azienda biotecnologica che sviluppa organi ingegnerizzati compatibili con l’uomo).
La razza di maiali in miniatura dello Yucatan è stata specificamente selezionata come donatore ideale, grazie alle dimensioni degli organi paragonabili a quelle umane.
I reni del modello suino sono stati in precedenza trapiantati nelle scimmie riportando una sopravvivenza fino a 2 anni.
maiali in miniatura dello Yucatan
 Gli esperimenti successivi prevedevano il trapianto dei reni ingegnerizzati in esseri umani in stato di morte cerebrale e poiché questi esperimenti hanno avuto un certo successo, ecco che l’équipe di trapianti dell’MGH ha, quindi, ritenuto che anche il paziente di 62 anni poteva rappresentare un candidato ideale per l’ innovativo intervento chirurgico. Da qui la richiesta per ottenere l’autorizzazione all’uso compassionevole da parte della Food and Drug Administration (FDA) statunitense.
Gli esperimenti successivi prevedevano il trapianto dei reni ingegnerizzati in esseri umani in stato di morte cerebrale e poiché questi esperimenti hanno avuto un certo successo, ecco che l’équipe di trapianti dell’MGH ha, quindi, ritenuto che anche il paziente di 62 anni poteva rappresentare un candidato ideale per l’ innovativo intervento chirurgico. Da qui la richiesta per ottenere l’autorizzazione all’uso compassionevole da parte della Food and Drug Administration (FDA) statunitense.
Immunosoppressione e prevenzione delle infezioni
Il regime immunosoppressivo utilizzato ha compreso l’anticorpo sperimentale tegoprubart, un anticorpo umanizzato anti-CD40 ligando dell’immunoglobulina IgG1, e ravulizumab, un altro anticorpo monoclonale approvato dalla FDA.
Tegoprubart, descritto come una pietra miliare nella immunomodulazione dei trapianti, ha dimostrato in precedenza di essere in grado di aumentare la vita funzionale degli organi xenotrapiantati, cioè degli organi di animali trapiantati nell’uomo.
Il farmaco è stato utilizzato nel regime di immunosoppressione del 2° trapianto di cuore da maiale ad uomo eseguito dall’University of Maryland Medical Center di Baltimora nel settembre 2023.
In quel caso, il paziente era morto due mesi dopo il trapianto. Al contrario, i chirurghi dell’MGH hanno, invece, dichiarato che il trapiantato di rene è risultato più sano dei due riceventi dei trapianti di cuore di maiale al NYU Langone Health, a dimostrazione che i reni funzionano meglio dei cuori.
Cuori e Reni suini
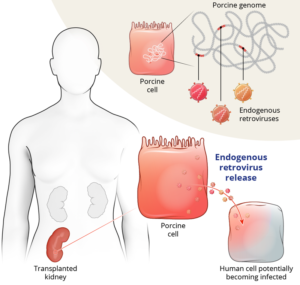
 Nel primo trapianto di cuore di maiale ingegnerizzato, infatti, si è scoperto che il cuore era stato infettato da un virus latente, mentre nei casi dei trapianti di rene nei primati non umani non sono state riscontrate malattie infettive derivate dai suini.
Nel primo trapianto di cuore di maiale ingegnerizzato, infatti, si è scoperto che il cuore era stato infettato da un virus latente, mentre nei casi dei trapianti di rene nei primati non umani non sono state riscontrate malattie infettive derivate dai suini.
Con l’incoraggiante sopravvivenza delle scimmie fino a 2 anni, la speranza è, oggi, che l’organo compatibile con l’uomo possa mostrare una sopravvivenza a lungo termine paragonabile a quella dello studio preclinico sui primati non umani e nel frattempo sono in programma altri trapianti utilizzando il modello suino.
Trapianti di organi suini senza necessità di immunosoppressione?
In prospettiva, eGenesis ha in preventivo la missione di sviluppare un organo compatibile con l’uomo che possa evitare l’immunosoppressione cioè produrre organi di donatori suini che non richiedano l’immunosoppressione. Questo sta a significare che i pazienti sottoposti a trapianto non dovranno più seguire un regime di farmaci che sopprimono il sistema immunitario per prevenire il rigetto e ciò richiederà una manipolazione genetica aggiuntiva ma per far questo occorre la necessità di dati umani per aiutare a definire l’aspetto dell’ingegneria genetica.
reni di 30 anni?
Il chirurgo Jayme E. Locke (Centro Trapianti presso l’Università dell’Alabama) a Birmingham, che ha partecipato ai precedenti trapianti di rene suino in pazienti in stato di morte cerebrale, sta portando avanti alcuni piani per procedere con il trapianto di rene utilizzando un modello suino ingegnerizzato e un regime di immunosoppressione diverso per avere una più lunga durata del trapianto di organi da donatore suino in modo che gli xenotrapianti possano durare per tutta la vita del ricevente. Si sa che i maiali possono vivere fino a 30 anni al di fuori della catena alimentare e pertanto la speranza è che il loro rene abbiano una durata di vita simile.
Meglio dei donatori umani?
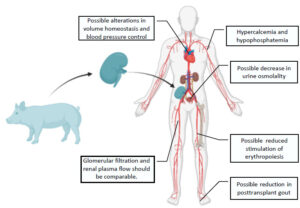
I reni suini geneticamente modificati potrebbero effettivamente rappresentare un miglioramento rispetto ai trapianti umani da cadavere per il fatto che con i donatori di rene umano a volte può capitare di trovarsi di fronte ad un ritardo nella funzione renale con il paziente bisognoso ancora di dialisi perché il rene non inizia a funzionare immediatamente. In altri casi, il rene potrebbe anche non recuperare mai la sua funzionalità.
In Italia, sono circa 6.000 i pazienti in attesa di trapianto di rene e di questi, si stima che circa 1 su 10 sia classificato come altamente sensibilizzato o iperimmunizzzato, ossia abbia sviluppato anticorpi contro la maggior parte degli antigeni HLA dei donatori.
Si ritiene che i tassi di ESKD risulteranno in notevole aumento entro il 2030 e considerata la necessità, il trapianto di rene da suino rappresenterebbe un evento molto incoraggiante per il campo della trapiantologia anche se c’è ancora molto lavoro da fare in termini di ulteriori studi clinici e di una attenta valutazione a lungo termine.
Bibliografia:
- Cooper DKC, Hara H, Iwase H et al (2021) “Pig kidney xenotransplantation: Progress toward clinical trials” . Clin Transplant. Jan; 35(1) : e 14139.
- Keith Reemtsma & al: “Renal Heterotransplantation in Man“; Ann Surg. 1964 Sep; 160(3): 384–408.
- Jagdale A, Kumar V, Anderson DJ et al. (2021) “Suggested Patient Selction Criteria for Initial Clinical Trials of Pig Kidney Xenotransplantation in the United States”. Transplantation Sep 1;105(9):1904 – 1908
- Anand RP et al ( 2023) “Design and testing of a humanized porcine donor for xenotransplantation“; Nature 622, 393 – 401 (2023)
- Porret PM et al (2022) “First clinical-grade porcine kidney xenotransplant using a human decedent model” Am J Transplant Apr; 22 (4) :1037 – 1053
- Tector AJ et al (2023) “Current Status of Renal Xenotransplantation and Next Steps”. Kidney360°, 4(2):278–284.
- Locke JE et al (2023) “Normal Graft Function After Pig-to-Human Kidney Xenotransplant”. JAMA Surg ;158(10):1106-1108
- Jones – Carr ME et al (2024) “C5 inhibition with eculizumab prevents thrombotic microangiopathy in a case series of pig-to-human kidney xenotransplantation”. J Clin Invest Mar 1; 134 (5)
Le foto sono state tratte dai siti: